Oltan® Amlo D 40/5/12,5 Comprimidos recubiertos
CLASIFICACIÓN
Antagonistas de la angiotensina II, bloqueadores de los canales del calcio y diuréticos.
COMPOSICIÓN Y PRESENTACIÓN
Composición: Cada comprimido recubierto contiene:
- Olmesartan medoxomilo 40,000 mg
- Amlodipino (como besilato) 5,000 mg
- Hidroclorotiazida 12,500 mg
Excipientes c.s.: Povidona, almidón de maíz pregelatinizado, celulosa microcristalina silicificada, lactosa monohidrato, estearato de magnesio, alcohol polivinílico, macrogol, dióxido de titanio, talco, Óxido de hierro amarillo.
Presentación: Envase con 30 comprimidos.
INDICACIONES
Tratamiento de la hipertensión esencial.
- Terapia complementaria: Oltan Amlo D 40/5/12,5 está indicado en pacientes adultos cuya presión arterial no está controlada adecuadamente con la combinación de olmesartán medoxomilo y amlodipino, administrado como formulación de dos componentes, en las mismas dosis.
- Terapia de sustitución: Oltan Amlo D 40/5/12,5 comprimidos recubiertos se indica como terapia de sustitución en pacientes adultos cuya presión arterial está controlada adecuadamente con la combinación de olmesartán medoxomilo, amlodipino e hidroclorotiazida, en las mismas dosis, administrado como un componente dual (olmesartán medoxomilo y amlodipino u olmesartán medoxomilo e hidroclorotiazida) y una formulación de un solo componente (hidroclorotiazida o amlodipino).
CONTRAINDICACIONES
Hipersensibilidad a los principios activos, a derivados de dihidropiridina o a sustancias derivadas de sulfonamida (dado que hidroclorotiazida es un fármaco derivado de sulfonamida), o a alguno de los excipientes de los comprimidos.
Insuficiencia renal grave.
Hipocalemia refractaria, hipercalcemia, hiponatremia e hiperuricemia sintomática.
Insuficiencia hepática grave, colestasis y trastornos obstructivos biliares.
2do y 3er trimestre del embarazo.
El uso concomitante de Oltan Amlo D 40/5/12,5 con productos que contienen aliskireno está contraindicado en pacientes con diabetes mellitus o deterioro renal (GFR <60 mL / min / 1,73 m2).
Debido al componente amlodipino, Oltan Amlo D 40/5/12,5 está contraindicado en pacientes con:
- Schock (incluido shock cardiogénico).
- Hipotensión severa.
- Obstrucción del tracto de salida del ventrículo izquierdo (por ejemplo, estenosis aórtica de alto grado).
- Insuficiencia cardíaca hemodinámicamente inestable luego de un infarto agudo de miocardio.
ADVERTENCIAS Y PRECAUCIONES
Antes de usar este medicamento debe sopesarse los riesgos y los beneficios de su uso, los que deben ser discutidos entre usted y su médico. Principalmente debe considerar los aspectos siguientes:
- Pacientes con hipovolemia o con depleción de sodio: La hipotensión sintomática puede ocurrir en pacientes que tienen un volumen y / o depleción de sodio como resultado de una terapia diurética vigorosa, restricción de sal en la dieta, diarrea o vómitos, especialmente después de la primera dosis.
Se recomienda la corrección de esta afección antes de la administración de Oltan Amlo D 40/5/12,5 o una estrecha supervisión médica al inicio del tratamiento. - Otras afecciones con estimulación del sistema renina-angiotensina-aldosterona: En pacientes cuyo tono vascular y función renal dependen predominantemente de la actividad del sistema renina-angiotensina- aldosterona (p. ej., pacientes con insuficiencia cardíaca congestiva grave o enfermedad renal subyacente, incluida la estenosis de la arteria renal), el tratamiento con medicamentos que afectan a este sistema se ha asociado con hipotensión aguda, azotemia, oliguria o, rara vez, insuficiencia renal aguda.
- Hipertensión Renovascular: Existe un mayor riesgo de hipotensión grave e insuficiencia renal cuando los pacientes con estenosis de la arteria renal bilateral o estenosis de la arteria de un único riñón funcional se tratan con medicamentos que afectan el sistema renina-angiotensina-aldosterona.
- Insuficiencia renal y trasplante renal: No se recomienda el uso de Oltan Amlo D 40/5/12,5 en pacientes con insuficiencia renal leve, moderada o grave (clearance de creatinina <30 mL / min).
La azotemia asociada a diuréticos tiazídicos puede ocurrir en pacientes con insuficiencia renal.
Si la insuficiencia renal progresiva se vuelve evidente, es necesaria una reevaluación cuidadosa de la terapia, considerando la interrupción de la terapia con diuréticos.
No hay experiencia en la administración de Olmesartán medoxomilo / Amlodipino / Hidroclorotiazida en pacientes con un trasplante renal reciente o en pacientes con insuficiencia renal terminal (es decir, clearance de creatinina <12 mL / min). - Bloqueo dual del sistema renina-angiotensina-aldosterona (RAAS): Existe evidencia de que el uso concomitante de inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren aumenta el riesgo de hipotensión, hipercalemia y disminuye la función renal (incluyendo insuficiencia renal aguda). Por lo tanto, no se recomienda el bloqueo dual de RAAS mediante el uso combinado de inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren.
Si la terapia de bloqueo dual se considera absolutamente necesaria, solo deberá ocurrir bajo la supervisión de un especialista y estar sujeta a una estrecha vigilancia de la función renal, electrolitos y presión arterial.
Los inhibidores de la ECA y los bloqueadores de los receptores de angiotensina II no deben usarse concomitantemente en pacientes con nefropatía diabética. - Insuficiencia hepática: La exposición a amlodipino y olmesartán medoxomilo aumenta en pacientes con insuficiencia hepática.
Además, las alteraciones menores del equilibrio de líquidos y electrolitos durante la terapia con tiazidas pueden precipitar el coma hepático en pacientes con insuficiencia hepática o enfermedad hepática progresiva.
Se debe tener cuidado cuando se administra Oltan Amlo D 40/5/12,5 en pacientes con insuficiencia hepática leve.
En pacientes con insuficiencia hepática moderada, la dosis de olmesartán medoxomilo no debe superar los 20 mg, por lo tanto, Oltan Amlo D 40/5/12,5 no está recomendado en esa población.
En pacientes con insuficiencia hepática, se debe iniciar el tratamiento en el extremo inferior del rango de dosificación de amlodipino y se debe tener precaución, tanto en el tratamiento inicial como al aumentar la dosis.
El uso de Olmesartán medoxomilo / Amlodipino / Hidroclorotiazida está contraindicado en pacientes con insuficiencia hepática grave, colestasis u obstrucción biliar. - Estenosis valvular aórtica y mitral, miocardiopatía hipertrófica obstructiva: Debido al componente amlodipino de Oltan Amlo D 40/5/12,5, como con otros vasodilatadores, se recomienda precaución especial en pacientes que sufren estenosis aórtica o mitral, o miocardiopatía hipertrófica obstructiva.
- Aldosteronismo primario: Los pacientes con aldosteronismo primario generalmente no responderán a los medicamentos antihipertensivos que actúan mediante la inhibición del sistema renina-angiotensina. Por lo tanto, el uso de Oltan Amlo D 40/5/12,5 no está recomendado en estos pacientes.
- Efectos metabólicos y endocrinos: La terapia con tiazidas puede afectar la tolerancia a la glucosa. En pacientes diabéticos, pueden requerirse ajustes de dosis de insulina o agentes hipoglucemiantes orales. La diabetes mellitus latente puede manifestarse durante la terapia con tiazidas.
Los aumentos en los niveles de colesterol y triglicéridos son efectos indeseables que se sabe están asociados con la terapia con diuréticos tiazídicos.
Puede producirse hiperuricemia o puede precipitarse gota en algunos pacientes que reciben terapia con tiazidas. - Desequilibrio electrolítico: Como para cualquier paciente que recibe terapia diurética, la determinación periódica de electrolitos séricos debe realizarse a intervalos apropiados.
Las tiazidas, incluida la hidroclorotiazida, pueden causar un desequilibrio de líquidos o electrolitos (incluyendo hipocalemia, hiponatremia y alcalosis hipoclorémica). Señales de advertencia de desbalance de fluidos o de electrolitos son la sequedad de boca, sed, debilidad, letargo, somnolencia, inquietud, dolor muscular o calambres, fatiga muscular, hipotensión, oliguria, taquicardia y trastornos gastrointestinales como náuseas o vómitos.
El riesgo de hipocalemia es mayor en pacientes con cirrosis hepática, en pacientes que experimentan diuresis enérgica, en pacientes que reciben una ingesta oral inadecuada de electrolitos y en pacientes que reciben terapia concomitante con corticosteroides o ACTH.
Por el contrario, debido al antagonismo en los receptores de angiotensina II (AT1) a través del componente olmesartán medoxomilo de Oltan Amlo D 40/5/12,5 pueden producirse hipercalemia, especialmente en presencia de insuficiencia renal y / o insuficiencia cardíaca, y diabetes mellitus. Se recomienda una estrecha monitorización del potasio sérico en pacientes en riesgo.
Los diuréticos ahorradores de potasio, los suplementos de potasio o los sustitutos de la sal que contienen potasio y otros medicamentos que pueden aumentar los niveles séricos de potasio (p. Ej., Heparina) deben administrarse con precaución junto con Oltan Amlo D 40/5/12,5 y con monitorización frecuente de los niveles de potasio.
No hay evidencia de que olmesartán medoxomilo reduzca o prevenga la hiponatremia inducida por diuréticos. El déficit de cloruro es generalmente leve y usualmente no requiere tratamiento.
Las tiazidas pueden disminuir la excreción urinaria de calcio y causar una elevación intermitente y leve del calcio sérico en ausencia de trastornos conocidos del metabolismo del calcio.
La hipercalcemia puede ser evidencia de hiperparatiroidismo oculto. Las tiazidas deben suspenderse antes de realizar pruebas para la función paratiroidea.
Se ha demostrado que las tiazidas aumentan la excreción urinaria de magnesio, lo que puede provocar hipomagnesemia.
La hiponatremia dilucional puede ocurrir en pacientes edematosos en climas cálidos. - Litio: Al igual que con otros antagonistas de los receptores de angiotensina II, no se recomienda la administración conjunta de Oltan Amlo D 40/5/12,5 con litio.
- Insuficiencia cardiaca: Como consecuencia de la inhibición del sistema renina-angiotensina-aldosterona, se pueden anticipar cambios en la función renal en individuos susceptibles.
En pacientes con insuficiencia cardíaca grave cuya función renal puede depender de la actividad del sistema renina – angiotensina – aldosterona, el tratamiento con inhibidores de la enzima convertidora de angiotensina (ECA) y antagonistas de los receptores de angiotensina se ha asociado con oliguria y / o azotemia progresiva y (raramente) con insuficiencia renal aguda y / o muerte.
Los pacientes con insuficiencia cardíaca deben ser tratados con precaución. En un estudio a largo plazo controlado con placebo de amlodipino en pacientes con insuficiencia cardíaca grave (NYHA III y IV), la incidencia informada de edema pulmonar fue mayor en el grupo de amlodipino que en el grupo placebo. Los bloqueadores de los canales de calcio, incluido el amlodipino, deben usarse con precaución en pacientes con insuficiencia cardíaca congestiva, ya que pueden aumentar el riesgo de futuros eventos cardiovasculares y mortalidad. - Enteropatía tipo Sprue: En casos muy raros, se ha informado diarrea crónica grave con pérdida de peso sustancial en pacientes que toman olmesartan meses o años después del inicio del fármaco, posiblemente causada por una reacción de hipersensibilidad retrasada localizada. Las biopsias intestinales de pacientes a menudo demostraron atrofia vellosa. Si un paciente desarrolla estos síntomas durante el tratamiento con olmesartan, y en ausencia de otras etiologías aparentes, el tratamiento con olmesartan debe suspenderse inmediatamente y no debe reiniciarse. Si la diarrea no mejora durante la semana posterior a la interrupción, se deben considerar otros consejos especializados (por ejemplo, un gastroenterólogo).
- Miopía aguda y glaucoma secundario de ángulo cerrado: La hidroclorotiazida, una sulfonamida, puede causar una reacción idiosincrásica, resultando en miopía transitoria aguda y glaucoma agudo de ángulo cerrado. Los síntomas incluyen un inicio agudo de disminución de la agudeza visual o dolor ocular y, por lo general, ocurren entre unas horas y semanas después del inicio del fármaco. El glaucoma agudo de ángulo cerrado no tratado puede conducir a una pérdida de visión permanente. El tratamiento primario es descontinuar hidroclorotiazida lo más rápido posible. Es posible que se deban considerar tratamientos médicos o quirúrgicos inmediatos si la presión intraocular permanece sin control. Los factores de riesgo para desarrollar glaucoma de ángulo cerrado agudo pueden incluir antecedentes de alergia a la sulfonamida o la penicilina.
- Embarazo: Los antagonistas de los receptores de angiotensina II no deben iniciarse durante el embarazo. A menos que la terapia continua de antagonistas de los receptores de angiotensina II se considere esencial, pacientes que planeen un embarazo deberán considerar su cambio a tratamientos antihipertensivos alternativos que tengan un perfil de seguridad establecido para su uso en el embarazo. Cuando se diagnostica el embarazo, el tratamiento con antagonistas de los receptores de angiotensina II debe
interrumpirse de inmediato y, si corresponde, se debe iniciar una terapia alternativa. - Población pediátrica: Olmesartán medoxomilo / Amlodipino / Hidroclorotiazida no está indicado en niños y adolescentes menores de 18 años.
- Ancianos: En los ancianos, el aumento de la dosis debe realizarse con cuidado.
- Fotosensibilidad: Se han notificado casos de reacciones de fotosensibilidad con diuréticos tiazídicos. Si se produce una reacción de fotosensibilidad durante el tratamiento con Oltan Amlo D 40/5/12,5, se recomienda suspender el tratamiento. Si se considera necesario volver a administrar el diurético, se recomienda proteger las áreas expuestas al sol o a los rayos UVA artificiales.
- Cáncer de piel no melanoma: Se ha observado un aumento del riesgo de cáncer de piel no melanoma (CPNM) [carcinoma de células basales (CBC) y carcinoma de células escamosas (CEC)] con el aumento de la dosis acumulativa de exposición a hidroclorotiazida (HCTZ) en dos estudios epidemiológicos basados en el Registro Nacional Danés de Cáncer.
Las acciones de fotosensibilización de hidroclorotiazida podrían actuar como un posible mecanismo para CPNM.
Consulte a su médico/farmacéutico/enfermero, antes de empezar a usar este producto; si ha tenido cáncer de piel o si le aparece una lesión de la piel inesperada durante el tratamiento. El tratamiento con hidroclorotiazida, en particular su uso a largo plazo a dosis altas puede aumentar el riesgo de algunos tipos de cáncer de piel y labios (cáncer de piel no-melanoma). Proteja la piel de la exposición al sol y a los rayos UV mientras esté tomando este medicamento.
Las lesiones cutáneas sospechosas deben examinarse de inmediato con la posibilidad de incluir exámenes histológicos de biopsias.
Es posible que sea necesario reconsiderar el uso de hidroclorotiazida en pacientes que han experimentado previamente CPNM. - Otros: Al igual que con cualquier agente antihipertensivo, la reducción excesiva de la presión arterial en pacientes con cardiopatía isquémica o enfermedad cerebrovascular isquémica podría provocar un infarto de miocardio o un accidente cerebrovascular.
Las reacciones de hipersensibilidad a la hidroclorotiazida pueden ocurrir en pacientes con o sin antecedentes de alergia o asma bronquial, pero son más probables en pacientes con dicho historial.
La exacerbación o activación del lupus eritematoso sistémico se ha informado con el uso de diuréticos tiazídicos.
Al igual que con todos los otros antagonistas del receptor de angiotensina II, el efecto reductor de la presión arterial de olmesartan es algo menor en pacientes negros que en pacientes no negros, sin embargo, este efecto no se observó en uno de los tres ensayos clínicos realizados con comprimidos de Olmesartán medoxomilo / Amlodipino / Hidroclorotiazida que incluyeron pacientes negros (30%). - Oltan Amlo D 40/5/12,5 contiene lactosa: Los pacientes con problemas hereditarios raros de intolerancia a la galactosa, deficiencia total de lactasa o malabsorción de glucosa-galactosa no deben tomar este medicamento.
Fertilidad, embarazo y lactancia
- Embarazo: El uso de la combinación de olmesartan medoxomilo / amlodipino / hidroclorotiazida está contraindicado durante el segundo y tercer trimestre del embarazo. Dados los efectos de los componentes individuales en este producto combinado durante el embarazo, no se recomienda el uso de Oltan Amlo D 40/5/12,5 durante el primer trimestre de embarazo.
- Olmesartan medoxomilo: No se recomienda el uso de antagonistas de los receptores de angiotensina II durante el primer trimestre del embarazo. El uso de antagonistas del receptor de angiotensina II está contraindicado durante el 2º y 3º trimestre del embarazo.
La evidencia epidemiológica sobre el riesgo de teratogenicidad después de la exposición a los inhibidores de la ECA durante el primer trimestre del embarazo no ha sido concluyente; sin embargo, un pequeño aumento en el riesgo no puede ser excluido. Si bien no hay datos epidemiológicos controlados sobre el riesgo con los antagonistas de los receptores de angiotensina II, pueden existir riesgos similares para esta clase de medicamentos. A menos que la terapia con bloqueadores del receptor de angiotensina continúe considerándose esencial, las pacientes que planean un embarazo deben cambiarse a tratamientos antihipertensivos alternativos, que tienen un perfil de seguridad establecido para su uso en el embarazo.
Cuando se diagnostica el embarazo, el tratamiento con antagonistas de los receptores de angiotensina II debe suspenderse de inmediato y, si corresponde, se debe iniciar una terapia alternativa.
Se sabe que la exposición a la terapia con antagonistas de los receptores de angiotensina II durante el segundo y tercer trimestres induce fetotoxicidad humana (disminución de la función renal, oligohidramnios, retraso de la osificación del cráneo) y toxicidad neonatal (insuficiencia renal, hipotensión, hipercalemia).
Si la exposición a los antagonistas de los receptores de angiotensina II ha ocurrido desde el segundo trimestre del embarazo, se recomienda realizar una ecografía de la función renal y del cráneo. Bebés, cuyas madres han tomado antagonistas de los receptores de angiotensina II deben observarse atentamente para detectar hipotensión. - Hidroclorotiazida: Existe una experiencia limitada con hidroclorotiazida durante el embarazo, especialmente durante el primer trimestre. Los estudios en animales son insuficientes.
Hidroclorotiazida atraviesa la placenta. Según el mecanismo de acción farmacológico de hidroclorotiazida, su uso durante el segundo y tercer trimestre puede comprometer la perfusión feto- placentaria y puede causar efectos fetales y neonatales como ictericia, alteración del equilibrio electrolítico y trombocitopenia.
Hidroclorotiazida no debe usarse para el edema gestacional, la hipertensión gestacional o la preeclampsia debido al riesgo de disminución del volumen plasmático y la hipoperfusión placentaria, sin un efecto beneficioso sobre el curso de la enfermedad.
Hidroclorotiazida no debe usarse para la hipertensión esencial en mujeres embarazadas, excepto en situaciones raras en las que no se pueda usar otro tratamiento. - Amlodipino: Los datos sobre un número limitado de embarazos expuestos no indican que amlodipino u otros antagonistas de los receptores de calcio tengan un efecto nocivo sobre la salud del feto. Sin embargo, puede haber un riesgo de parto prolongado.
- Olmesartan medoxomilo: No se recomienda el uso de antagonistas de los receptores de angiotensina II durante el primer trimestre del embarazo. El uso de antagonistas del receptor de angiotensina II está contraindicado durante el 2º y 3º trimestre del embarazo.
- Lactancia: Durante la lactancia, la combinación de olmesartan medoxomilo / amlodipino / hidroclorotiazida no es recomendada y son preferibles tratamientos alternativos con mejores perfiles de seguridad establecidos durante la lactancia, especialmente durante la lactancia de un recién nacido o un bebé prematuro.
Olmesartan se excreta en la leche de las ratas lactantes. Sin embargo, no se sabe si el olmesartan pasa a la leche humana.
Amlodipino se excreta en la leche humana. La proporción de la dosis materna recibida por el lactante se ha estimado con un rango intercuartil del 3 al 7%, con un máximo del 15%. El efecto de amlodipino se desconoce en lactantes.
Hidroclorotiazida se excreta en la leche humana en pequeñas cantidades. Las tiazidas en dosis altas causan diuresis intensa que pueden inhibir la producción de leche.
No se recomienda el uso de la combinación de olmesartan medoxomilo / amlodipino / hidroclorotiazida durante la lactancia. Si se usa Oltan Amlo D 40/5/12,5 durante la lactancia, las dosis deben mantenerse lo más bajas posible. - Fertilidad: Se han informado cambios bioquímicos reversibles en la cabeza de los espermatozoides en algunos pacientes tratados con bloqueadores de los canales de calcio.
Los datos clínicos son insuficientes con respecto al posible efecto de amlodipino sobre la fertilidad. En un estudio con ratas, se encontraron efectos adversos sobre la fertilidad masculina.
Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios sobre los efectos y la capacidad para conducir y utilizar máquinas.
Sin embargo, debe tenerse en cuenta que los pacientes que toman terapia antihipertensiva pueden ocasionar mareos, dolor de cabeza, náuseas o fatiga y que estos síntomas pueden afectar la capacidad de reacción. Se recomienda precaución especialmente al inicio del tratamiento.
INTERACCIONES
Interacciones potenciales relacionadas con la combinación de Olmesartan medoxomilo / Amlodipino / Hidroclorotiazida:
- Uso concomitante no recomendado
- Litio: Aumentos reversibles en las concentraciones séricas de litio y toxicidad se han reportado durante la administración concomitante de litio con inhibidores de la enzima convertidora de angiotensina y, raramente, con antagonistas de los receptores de angiotensina II. Además, las tiazidas reducen el clearance renal de litio y, en consecuencia, puede aumentar el riesgo de toxicidad por litio. Por lo tanto, no se recomienda el uso de la combinación olmesartan medoxomilo / amlodipino / hidroclorotiazida y litio.
Si el uso de la combinación resulta necesario, se recomienda un control cuidadoso de los niveles séricos de litio.
- Litio: Aumentos reversibles en las concentraciones séricas de litio y toxicidad se han reportado durante la administración concomitante de litio con inhibidores de la enzima convertidora de angiotensina y, raramente, con antagonistas de los receptores de angiotensina II. Además, las tiazidas reducen el clearance renal de litio y, en consecuencia, puede aumentar el riesgo de toxicidad por litio. Por lo tanto, no se recomienda el uso de la combinación olmesartan medoxomilo / amlodipino / hidroclorotiazida y litio.
- Uso concomitante que requiere precaución
- Baclofeno: Se puede producir la potenciación del efecto antihipertensivo.
- Medicamentos antiinflamatorios no esteroideos: Los AINEs (es decir, ácido acetilsalicílico (> 3 g / día), inhibidores de la COX-2 y AINEs no selectivos) pueden reducir el efecto antihipertensivo de los diuréticos tiazídicos y los antagonistas de los receptores de angiotensina II.
En algunos pacientes con función renal comprometida (por ejemplo, pacientes deshidratados o personas de edad avanzada con función renal comprometida), la administración conjunta de antagonistas y agentes del receptor de angiotensina II que inhiben la ciclooxigenasa puede provocar un mayor deterioro de la función renal, incluida una posible insuficiencia renal aguda, que generalmente es reversible. Por lo tanto, la combinación debe administrarse con precaución, especialmente en los ancianos. Los pacientes deben estar adecuadamente hidratados y se debe considerar la monitorización de la función renal después del inicio de la terapia concomitante como también periódicamente después.
- Uso concomitante a tener en cuenta
- Amifostina: Se puede producir la potenciación del efecto antihipertensivo.
- Otros agentes antihipertensivos: El efecto reductor de la presión arterial de la combinación de olmesartán medoxomilo / amlodipino / hidroclorotiazida puede verse aumentado con el uso concomitante de otros medicamentos antihipertensivos.
- Alcohol, barbitúricos, narcóticos o antidepresivos: La potenciación de la hipotensión ortostática puede ocurrir.
Posibles interacciones relacionadas con Olmesartan medoxomilo
- Uso concomitante no recomendado
- Inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren: Los datos de los ensayos clínicos han demostrado que el bloqueo dual del sistema renina-angiotensina-aldosterona (RAAS) mediante el uso combinado de inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren se asocia con una mayor frecuencia de eventos adversos como hipotensión, hipercalemia y disminución de la función renal (incluida la insuficiencia renal aguda) en comparación con el uso de un único agente de acción RAAS.
- Medicamentos que afectan los niveles de potasio: El uso concomitante de diuréticos ahorradores de potasio, suplementos de potasio, sustitutos de la sal que contengan potasio u otros medicamentos que pueden aumentar los niveles séricos de potasio (p. Ej., Heparina, inhibidores de la ECA) puede provocar un aumento del potasio sérico. Si los medicamentos que afectan el potasio se prescriben en combinación con Olmesartan medoxomilo / Amlodipino /
Hidroclorotiazida, se recomienda monitorizar el potasio sérico.
- Información Adicional
- Agente secuestrante de ácidos biliares colesevelam: La administración concurrente del agente secuestrante de ácidos biliares clorhidrato de colesevelam reduce la exposición sistémica y la concentración plasmática máxima de olmesartan y reduce t1/2. La administración de olmesartan medoxomilo al menos 4 horas antes del clorhidrato de colesevelam disminuyó el efecto de interacción farmacológica. Se debe considerar la administración de olmesartan medoxomilo al menos 4 horas antes de la dosis de clorhidrato de colesevelam.
Después del tratamiento con antiácidos (hidróxido de aluminio y magnesio), se observó una modesta reducción en la biodisponibilidad de olmesartan.
Olmesartan medoxomilo no tuvo un efecto significativo sobre la farmacocinética o farmacodinámica de la warfarina o la farmacocinética de la digoxina.
La administración conjunta de olmesartan medoxomilo con pravastatina no tuvo efectos clínicamente relevantes sobre la farmacocinética de ninguno de los componentes en sujetos sanos.
El olmesartan no tuvo efectos inhibitorios clínicamente relevantes sobre las enzimas citocromo P450 humanas 1A1/2, 2A6, 2C8/9, 2C19, 2D6, 2E1 y 3A4 in vitro, y no tuvo o indujo mínimos efectos inductores la actividad del citocromo P450 en ratas. No se esperan interacciones clínicamente relevantes entre olmesartan y medicamentos metabolizados por las enzimas citocromo P450 anteriores.
- Agente secuestrante de ácidos biliares colesevelam: La administración concurrente del agente secuestrante de ácidos biliares clorhidrato de colesevelam reduce la exposición sistémica y la concentración plasmática máxima de olmesartan y reduce t1/2. La administración de olmesartan medoxomilo al menos 4 horas antes del clorhidrato de colesevelam disminuyó el efecto de interacción farmacológica. Se debe considerar la administración de olmesartan medoxomilo al menos 4 horas antes de la dosis de clorhidrato de colesevelam.
Posibles interacciones relacionadas con amlodipino
- Uso concomitante que requiere precaución
- Efectos de otros medicamentos sobre amlodipino
Inhibidores de CYP3A4:
El uso concomitante de amlodipino con inhibidores potentes o moderados del CYP3A4 (inhibidores de la proteasa, antifúngicos azólicos, macrólidos como la eritromicina o claritromicina, verapamilo o diltiazem) puede dar lugar a un aumento significativo de la exposición a amlodipino. La traducción clínica de estas variaciones farmacocinéticas puede ser más pronunciada en los ancianos. Existe un mayor riesgo de hipotensión. Se recomienda una estrecha observación de los pacientes y, por lo tanto, puede ser necesario un ajuste de la dosis.
Inductores CYP3A4:
Tras la administración conjunta de inductores conocidos del CYP3A4, la concentración plasmática de amlodipino puede variar. Por lo tanto, se debe controlar la presión arterial y considerar la regulación de la dosis durante y después de la medicación concomitante, particularmente con inductores potentes de CYP3A4 (por ejemplo, rifampicina, hipericum perforatum).
No se recomienda la administración de amlodipino con pomelo o jugo de pomelo, ya que la biodisponibilidad puede aumentar en algunos pacientes, aumentando la disminución de la presión arterial.
Dantroleno (infusión): en animales, se observa fibrilación ventricular letal y colapso cardiovascular en asociación con hipercalemia después de la administración de verapamilo y dantroleno intravenoso.
dantrolene Debido al riesgo de hipercalemia, se recomienda evitar la administración conjunta de bloqueadores de los canales de calcio, como amlodipino, en pacientes susceptibles de hipertermia maligna y en el manejo de la hipertermia maligna. - Efectos de amlodipino sobre otros medicamentos.
El efecto reductor de la presión arterial de amlodipino se suma a los efectos reductores de la presión arterial de otros agentes antihipertensivos.
En estudios de interacción clínica, amlodipino no afectó la farmacocinética de atorvastatina, digoxina o warfarina.
Simvastatina: la administración conjunta de dosis múltiples de 10 mg de amlodipino con 80 mg de simvastatina resultó en un aumento del 77% en la exposición a la simvastatina en comparación con la simvastatina sola. Limite la dosis de simvastatina en pacientes con amlodipino a 20 mg diarios.
Tacrolimus: existe un riesgo de aumento de los niveles sanguíneos de tacrolimus cuando se administra conjuntamente con amlodipino. Para evitar la toxicidad de tacrolimus, la administración de amlodipino en un paciente tratado con tacrolimus requiere monitoreo de los niveles sanguíneos de tacrolimus y ajuste de dosis de tacrolimus cuando sea apropiado.
Ciclosporina: en un estudio prospectivo en pacientes con trasplante renal, se observó un aumento promedio del 40% en los niveles mínimos de ciclosporina cuando se usa concomitantemente con amlodipino. La coadministración de olmesartán medoxomilo / amlodipino / hidroclorotiazida con ciclosporina puede aumentar la exposición a la ciclosporina. Monitorear los niveles mínimos de ciclosporina durante el uso concomitante y las reducciones de dosis de ciclosporina se deben realizar según sea necesario.
- Efectos de otros medicamentos sobre amlodipino
Posibles interacciones relacionadas con la hidroclorotiazida
- Uso concomitante no recomendado
- Medicamentos que afectan los niveles de potasio: El efecto de reducción de potasio de la hidroclorotiazida puede verse potenciado por la administración conjunta de otros medicamentos asociados con la pérdida de potasio e hipocalemia (p. Ej. otros diuréticos kaliuréticos, laxantes, corticosteroides, ACTH, anfotericina, carbenoxolona, penicilina G sódica o derivados del ácido salicílico). Tal uso concomitante, por lo tanto, no se recomienda.
- Uso concomitante que requiere precaución
- Sales de calcio: Los diuréticos tiazídicos pueden aumentar el calcio sérico debido a la disminución de la excreción. Si se deben recetar suplementos de calcio, se debe controlar el calcio sérico y ajustar la dosis de calcio en consecuencia.
- Colestiramina y resinas de colestipol: La absorción de hidroclorotiazida se ve afectada en presencia de resinas de intercambio aniónico.
- Glucósidos digitálicos: La hipocalemia y la hipomagnesemia inducidas por tiazidas pueden favorecer la aparición de arritmias cardíacas inducidas por digital.
- Medicamentos afectados por trastornos séricos de potasio: Se recomienda la monitorización periódica del potasio sérico y el ECG cuando la combinación olmesartan medoxomilo / amlodipino / hidroclorotiazida se administra con medicamentos afectados por alteraciones séricas de potasio (por ejemplo, glucósidos y antiarrítmicos de digital) y con los siguientes medicamentos inductores de torsades de pointes (taquicardia ventricular) (incluidos algunos antiarrítmicos), siendo la hipocalemia un factor predisponente para torsades de pointes (taquicardia ventricular).
- Antiarrítmicos de clase Ia (por ejemplo, quinidina, hidroquinidina, disopiramida).
- Antiarrítmicos de clase III (por ejemplo, amiodarona, sotalol, dofetilida, ibutilida).
- Algunos antipsicóticos (por ejemplo, tioridazina, clorpromazina, levomepromazina, trifluoperazina, ciamemazina, sulpirida, sultoprida, amisulprida, tiaprida, pimozida, haloperidol, droperidol).
- Otros (por ejemplo, bepridil, cisaprida, difemanil, eritromicina IV, halofantrina, mizolastina, pentamidina, sparfloxacina, terfenadina, vincamina IV).
- Relajantes del músculo esquelético no despolarizantes (por ejemplo, tubocurarina): Hidroclorotiazida puede potenciar el efecto de los relajantes del músculo esquelético no despolarizantes.
- Agentes anticolinérgicos (por ejemplo, atropina, biperideno): Aumento de la biodisponibilidad de los diuréticos de tipo tiazida al disminuir la motilidad gastrointestinal y la tasa de vaciado del estómago.
- Medicamentos antidiabéticos (agentes orales e insulina): El tratamiento con una tiazida puede influir en la tolerancia a la glucosa. Puede ser necesario ajustar la dosis del medicamento antidiabético.
- Metformina: Metformina debe usarse con precaución debido al riesgo de acidosis láctica inducida por una posible insuficiencia renal funcional relacionada con la hidroclorotiazida.
- Betabloqueantes y diazóxido: Las tiazidas pueden potenciar el efecto hiperglucémico de los betabloqueantes y el diazóxido.
- Aminas presoras (por ejemplo, noradrenalina): El efecto de las aminas presoras puede disminuir.
- Medicamentos utilizados en el tratamiento de la gota (por ejemplo, probenecid, sulfinpirazona y alopurinol): Puede ser necesario ajustar la dosis de los medicamentos uricosúricos ya que hidroclorotiazida puede elevar el nivel de ácido úrico sérico. El aumento de la dosis de probenecid o sulfinpirazona puede ser necesario. La administración conjunta de una tiazida puede aumentar la incidencia de reacciones de hipersensibilidad al alopurinol.
- Amantadina: Las tiazidas pueden aumentar el riesgo de efectos adversos causados por amantadina.
- Agentes citotóxicos (por ejemplo, ciclofosfamida, metotrexato): Las tiazidas pueden reducir la excreción renal de medicamentos citotóxicos y potenciar sus efectos mielosupresores.
- Salicilatos: En caso de altas dosis de salicilatos, hidroclorotiazida puede aumentar el efecto tóxico de los salicilatos en el sistema nervioso central.
- Metildopa: Ha habido informes aislados de anemia hemolítica que ocurre con el uso concomitante de hidroclorotiazida y metildopa.
- Ciclosporina: El tratamiento concomitante con ciclosporina puede aumentar el riesgo de hiperuricemia y complicaciones de tipo gota.
- Tetraciclinas: La administración concomitante de tetraciclinas y tiazidas aumenta el riesgo de aumento de urea inducido por tetraciclina. Esta interacción probablemente no sea aplicable a la doxiciclina.
PRESENCIA DE OTRAS ENFERMEDADES
Interacciones potenciales relacionadas con la combinación de Olmesartan medoxomilo / Amlodipino / Hidroclorotiazida:
- Uso concomitante no recomendado
- Litio: Aumentos reversibles en las concentraciones séricas de litio y toxicidad se han reportado durante la administración concomitante de litio con inhibidores de la enzima convertidora de angiotensina y, raramente, con antagonistas de los receptores de angiotensina II. Además, las tiazidas reducen el clearance renal de litio y, en consecuencia, puede aumentar el riesgo de toxicidad por litio. Por lo tanto, no se recomienda el uso de la combinación olmesartan medoxomilo / amlodipino / hidroclorotiazida y litio.
Si el uso de la combinación resulta necesario, se recomienda un control cuidadoso de los niveles séricos de litio.
- Litio: Aumentos reversibles en las concentraciones séricas de litio y toxicidad se han reportado durante la administración concomitante de litio con inhibidores de la enzima convertidora de angiotensina y, raramente, con antagonistas de los receptores de angiotensina II. Además, las tiazidas reducen el clearance renal de litio y, en consecuencia, puede aumentar el riesgo de toxicidad por litio. Por lo tanto, no se recomienda el uso de la combinación olmesartan medoxomilo / amlodipino / hidroclorotiazida y litio.
- Uso concomitante que requiere precaución
- Baclofeno: Se puede producir la potenciación del efecto antihipertensivo.
- Medicamentos antiinflamatorios no esteroideos: Los AINEs (es decir, ácido acetilsalicílico (> 3 g / día), inhibidores de la COX-2 y AINEs no selectivos) pueden reducir el efecto antihipertensivo de los diuréticos tiazídicos y los antagonistas de los receptores de angiotensina II.
En algunos pacientes con función renal comprometida (por ejemplo, pacientes deshidratados o personas de edad avanzada con función renal comprometida), la administración conjunta de antagonistas y agentes del receptor de angiotensina II que inhiben la ciclooxigenasa puede provocar un mayor deterioro de la función renal, incluida una posible insuficiencia renal aguda, que generalmente es reversible. Por lo tanto, la combinación debe administrarse con precaución, especialmente en los ancianos. Los pacientes deben estar adecuadamente hidratados y se debe considerar la monitorización de la función renal después del inicio de la terapia concomitante como también periódicamente después.
- Uso concomitante a tener en cuenta
- Amifostina: Se puede producir la potenciación del efecto antihipertensivo.
- Otros agentes antihipertensivos: El efecto reductor de la presión arterial de la combinación de olmesartán medoxomilo / amlodipino / hidroclorotiazida puede verse aumentado con el uso concomitante de otros medicamentos antihipertensivos.
- Alcohol, barbitúricos, narcóticos o antidepresivos: La potenciación de la hipotensión ortostática puede ocurrir.
Posibles interacciones relacionadas con Olmesartan medoxomilo:
- Uso concomitante no recomendado
- Inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren: Los datos de los ensayos clínicos han demostrado que el bloqueo dual del sistema renina-angiotensina-aldosterona (RAAS) mediante el uso combinado de inhibidores de la ECA, bloqueadores de los receptores de angiotensina II o aliskiren se asocia con una mayor frecuencia de eventos adversos como hipotensión, hipercalemia y disminución de la función renal (incluida la insuficiencia renal aguda) en comparación con el uso de un único agente de acción RAAS.
- Medicamentos que afectan los niveles de potasio: El uso concomitante de diuréticos ahorradores de potasio, suplementos de potasio, sustitutos de la sal que contengan potasio u otros medicamentos que pueden aumentar los niveles séricos de potasio (p. Ej., Heparina, inhibidores de la ECA) puede provocar un aumento del potasio sérico. Si los medicamentos que afectan el potasio se prescriben en combinación con Olmesartan medoxomilo / Amlodipino /
Hidroclorotiazida, se recomienda monitorizar el potasio sérico.
- Información Adicional
- Agente secuestrante de ácidos biliares colesevelam: La administración concurrente del agente secuestrante de ácidos biliares clorhidrato de colesevelam reduce la exposición sistémica y la concentración plasmática máxima de olmesartan y reduce t1/2. La administración de olmesartan medoxomilo al menos 4 horas antes del clorhidrato de colesevelam disminuyó el efecto de interacción farmacológica. Se debe considerar la administración de olmesartan medoxomilo al menos 4 horas antes de la dosis de clorhidrato de colesevelam.
Después del tratamiento con antiácidos (hidróxido de aluminio y magnesio), se observó una modesta reducción en la biodisponibilidad de olmesartan.
Olmesartan medoxomilo no tuvo un efecto significativo sobre la farmacocinética o farmacodinámica de la warfarina o la farmacocinética de la digoxina.
La administración conjunta de olmesartan medoxomilo con pravastatina no tuvo efectos clínicamente relevantes sobre la farmacocinética de ninguno de los componentes en sujetos sanos.
El olmesartan no tuvo efectos inhibitorios clínicamente relevantes sobre las enzimas citocromo P450 humanas 1A1/2, 2A6, 2C8/9, 2C19, 2D6, 2E1 y 3A4 in vitro, y no tuvo o indujo mínimos efectos inductores la actividad del citocromo P450 en ratas. No se esperan interacciones clínicamente relevantes entre olmesartan y medicamentos metabolizados por las enzimas citocromo P450 anteriores.
- Agente secuestrante de ácidos biliares colesevelam: La administración concurrente del agente secuestrante de ácidos biliares clorhidrato de colesevelam reduce la exposición sistémica y la concentración plasmática máxima de olmesartan y reduce t1/2. La administración de olmesartan medoxomilo al menos 4 horas antes del clorhidrato de colesevelam disminuyó el efecto de interacción farmacológica. Se debe considerar la administración de olmesartan medoxomilo al menos 4 horas antes de la dosis de clorhidrato de colesevelam.
Posibles interacciones relacionadas con amlodipino:
- Uso concomitante que requiere precaución
- Efectos de otros medicamentos sobre amlodipino
PRESENCIA DE OTRAS ENFERMEDADES
Ver sección ADVERTENCIAS Y PRECAUCIONES.
EFECTOS ADVERSOS (NO DESEADOS)
Los medicamentos pueden producir algunos efectos no deseados además de los que se pretende obtener. Algunos de estos efectos pueden requerir atención médica.
Consulte inmediatamente al médico si presenta algunos de los síntomas siguientes:
- La seguridad de la combinación de olmesartan medoxomilo / amlodipino / hidroclorotiazida se investigó en ensayos clínicos en 7826 pacientes que recibieron olmesartan medoxomilo en combinación con amlodipino e hidroclorotiazida.
- Las reacciones adversas de los ensayos clínicos, los estudios de seguridad posteriores a la autorización y los informes espontáneos se resumen en la tabla 1 para la combinación de olmesartan medoxomilo / amlodipino / hidroclorotiazida, así como para los componentes individuales olmesartan medoxomilo, amlodipino e hidroclorotiazida en función del perfil de seguridad conocido de los componentes individuales.
- Las reacciones adversas notificadas con mayor frecuencia durante el tratamiento con olmesartan medoxomilo / amlodipino / hidroclorotiazida son edema periférico, dolor de cabeza y mareos.
- Se han utilizado las siguientes terminologías para clasificar la aparición de efectos no deseados:
- Muy común (≥1 / 10)
- Común (≥1 / 100 a <1/10)
- Poco común (≥1 / 1.000 a <1/100)
- Raras (≥1 / 10.000 a <1 / 1,000)
- Muy raro (<1 / 10.000)
- Desconocido (no puede estimarse a partir de los datos disponibles)
Tabla 1: Resumen de las reacciones adversas con olmesartan medoxomilo / amlodipino / hidroclorotiazida y los componentes individuales.
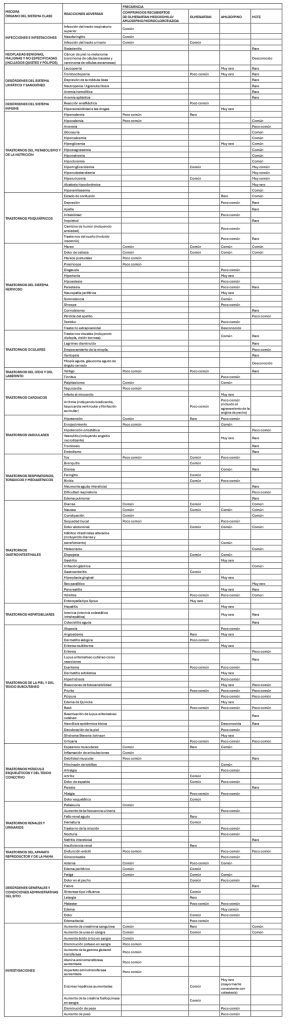
Se han notificado casos únicos de rabdomiólisis en asociación temporal con la ingesta de bloqueadores de los receptores de angiotensina II. Se han notificado casos únicos de síndrome extrapiramidal en pacientes tratados con amlodipino.
Cáncer de piel no melanoma
Según los datos disponibles de estudios epidemiológicos, se ha observado una asociación acumulativa dependiente de la dosis entre HCTZ y CPNM.
Sobredosis
- Síntomas
La dosis máxima de comprimidos recubiertos de Olmesartán medoxomilo / Amlodipino / Hidroclorotiazida es de 40 mg / 10 mg / 25 mg una vez al día. No hay información sobre sobredosis con olmesartan
medoxomilo / amlodipino / hidroclorotiazida en humanos. El efecto más probable de una sobredosis de olmesartan medoxomilo / amlodipino / hidroclorotiazida es la hipotensión.
Los efectos más probables de la sobredosis de olmesartan medoxomilo son hipotensión y taquicardia; se puede encontrar bradicardia si se produce estimulación parasimpática (vagal).
Se puede esperar que la sobredosis de amlodipino conduzca a una vasodilatación periférica excesiva con marcada hipotensión y posiblemente una taquicardia refleja. Se ha informado de hipotensión sistémica marcada y potencialmente prolongada, que puede incluir shock con desenlace fatal.
La sobredosis con hidroclorotiazida se asocia con el agotamiento de electrolitos (hipocalemia, hipocloremia) y la deshidratación resultante de una diuresis excesiva.
Los signos y síntomas más comunes de sobredosis son náuseas y somnolencia. La hipopotasemia puede provocar espasmos musculares y / o acentuar las arritmias cardíacas asociadas con el uso concomitante de glucósidos digitálicos o ciertos medicamentos antiarrítmicos. - Tratamiento
En caso de sobredosis de Oltan Amlo D 40/5/12,5, el tratamiento debe ser sintomático y de apoyo. El manejo depende del tiempo transcurrido desde la ingestión y la gravedad de los síntomas.
Si la ingesta es reciente, se puede considerar el lavado gástrico. En sujetos sanos, se ha demostrado que la administración de carbón activado inmediatamente o hasta 2 horas después de la ingestión de amlodipino reduce sustancialmente la absorción de amlodipino.
Hipotensión clínicamente significativa debido a una sobredosis de olmesartán medoxomilo / amlodipino / hidroclorotiazida requiere un apoyo activo del sistema cardiovascular, que incluye una estrecha monitorización de la función cardíaca y pulmonar, la elevación de las extremidades y atención al volumen de fluido circulante y producción de orina. Un vasoconstrictor puede ser útil para restaurar el tono vascular y la presión arterial, siempre que no haya contraindicaciones para su uso. Gluconato de calcio intravenoso puede ser beneficioso para revertir los efectos del bloqueo del canal de calcio.
Los electrolitos séricos y la creatinina deben controlarse con frecuencia. Si se produce hipotensión, el paciente debe colocarse en posición supina, con reposición de sal y volumen rápidamente.
Debido a que amlodipino está altamente unido a proteínas, no es probable que la diálisis sea beneficiosa. Se desconoce la dializabilidad de olmesartan o hidroclorotiazida.
No se ha establecido el grado en que olmesartan y la hidroclorotiazida se eliminan mediante hemodiálisis.
FORMA DE ADMINISTRACIÓN
El médico debe indicar la posología y el tiempo de tratamiento apropiado a su caso particular, no obstante, la dosis usual recomendada es de:
Adultos: La dosis recomendada de Oltan Amlo D 40/5/12,5 es de un comprimido recubierto al día.
El comprimido debe tragarse con una cantidad suficiente de líquido (por ejemplo, un vaso de agua). El comprimido no debe masticarse y debe tomarse a la misma hora todos los días.
Oltan Amlo D 40/5/12,5 comprimidos recubiertos puede tomarse con o sin comida.
CONDICIONES Y ALMACENAMIENTO
Mantener lejos del alcance de los niños, conservar en su envase original a menos de 25°C
No usar este producto después de la fecha de vencimiento indicada en el envase.
NO REPITA EL TRATAMIENTO SIN INDICACIÓN MEDICA
NO RECOMIENDE ESTE MEDICAMENTO A OTRA PERSONA